Soal Evaluasi
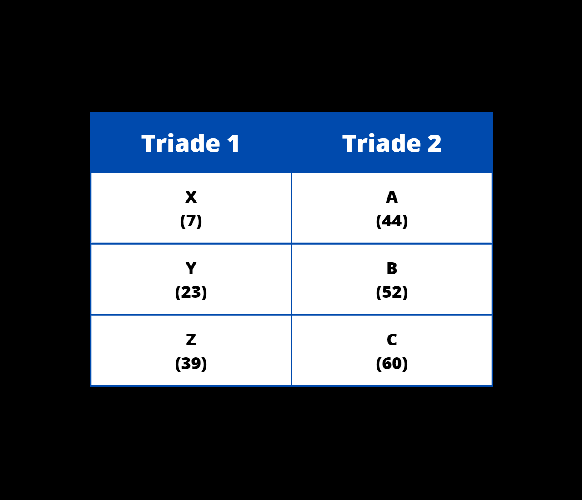
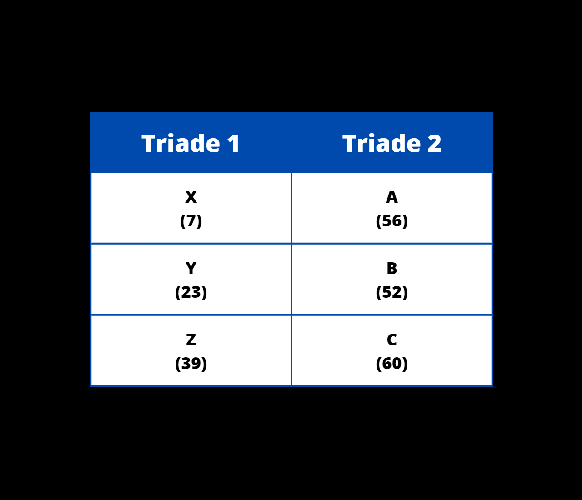
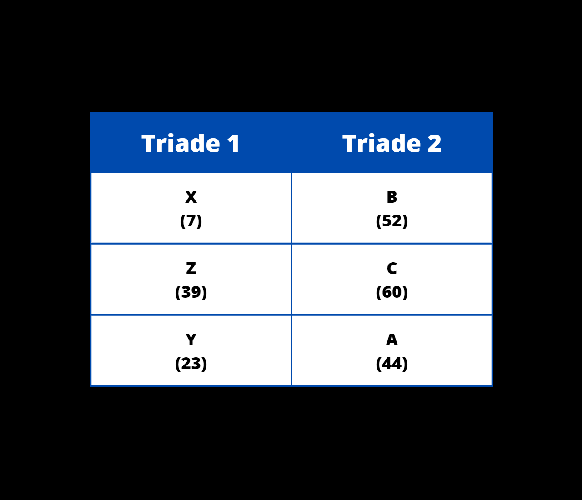
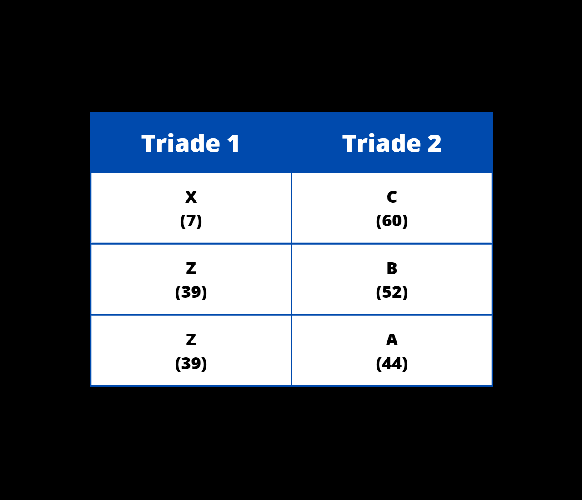
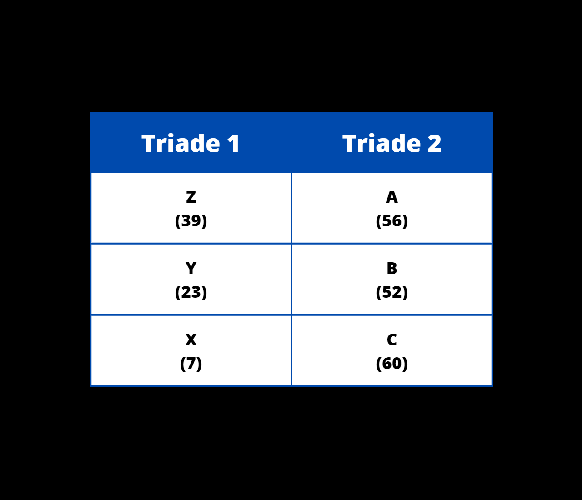
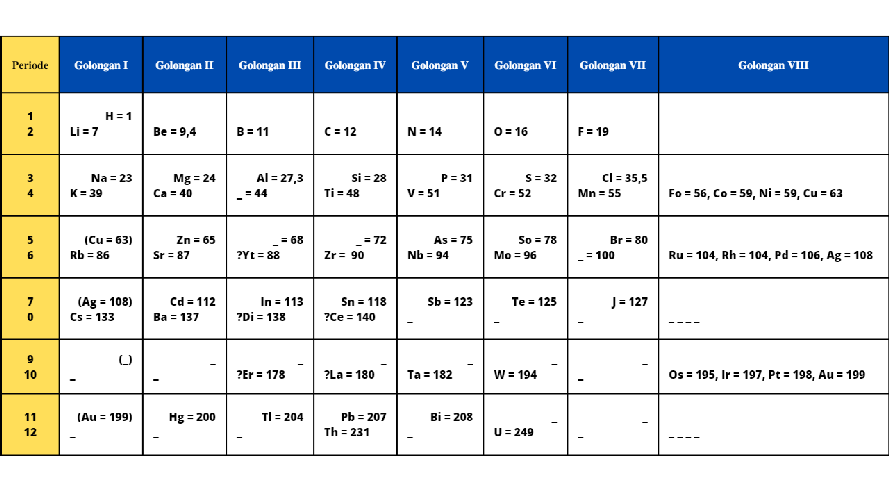
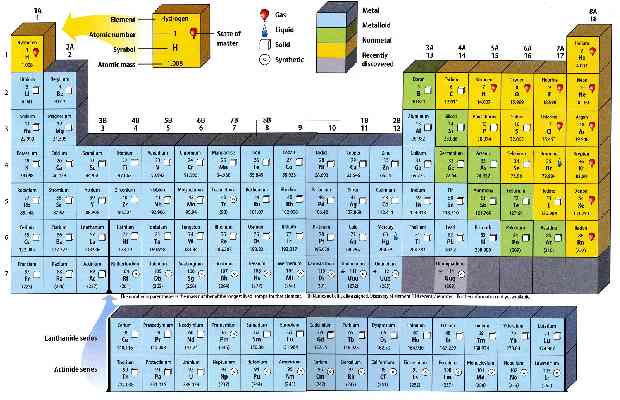
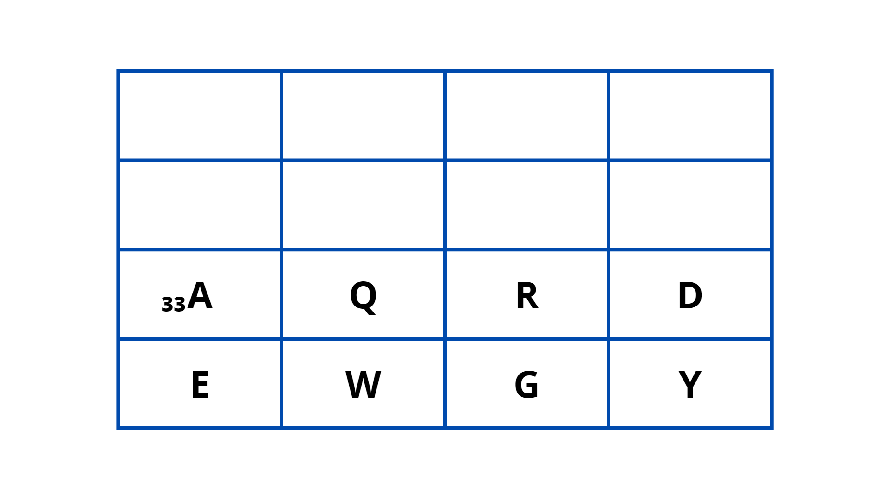
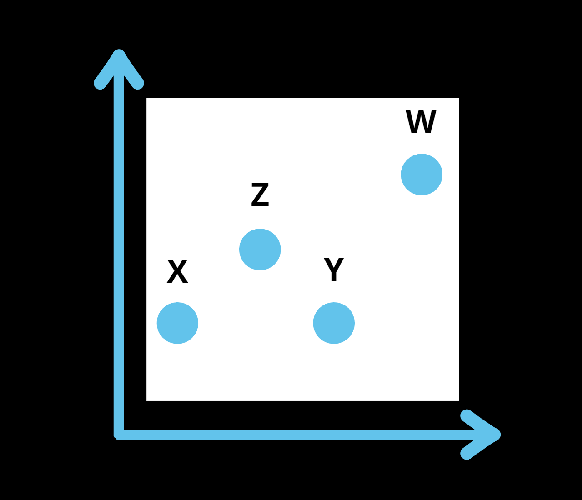
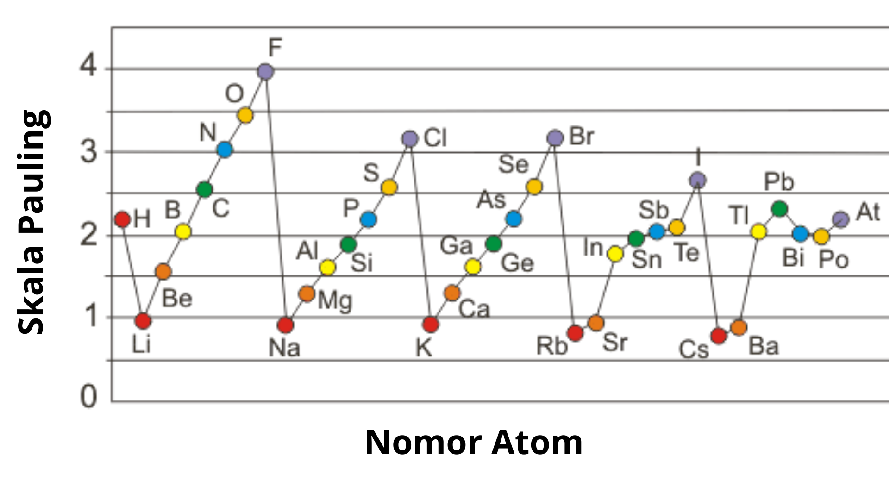
{"name":"Soal Evaluasi", "url":"https://www.quiz-maker.com/QPREVIEW","txt":"Pada Triade Dobereiner, unsur-unsur disusun berdasarkan triadnya. Apabila diketahui pada triade 1 (secara berturut-turt) terdapat unsur X, Y, Z dengan nomor massa X sebesar 7 dan nomor massa Z sebesar 39. Selanjutnya pada triade 2 (secara berturut-turut) terdapat unsur A, B, C dengan nomor massa B sebesar 52 dan nomor massa C sebesar 60. Berdasarkan uraian tersebut susunan Triade Dobereiner yang tepat adalah…., Perhatikan gambar berikut! Berdasarkan tabel tersebut, keunggulan dari periodik unsur Mendeleev adalah…, Perhatikan gambar berikut! Berdasarkan gambar tersebut, apabila terdapat unsur X yang memiliki sifat kimia serupa dengan Nitrogen (N) dan Bismut (Bi). Unsur X ini memiliki massa atom lebih besar daripada unsur Aluminium (Al), tetapi lebih kecil daripada Germanium (Ge). Letak unsur X tersebut pada tabel periodik adalah....","img":"https://www.quiz-maker.com/3012/images/ogquiz.png"}
More Surveys
Mornington peninsula Quiz!
10514
Covid Exposure Response questionnaire: TherapyWorx Building
4219
کانال خرید و فروش ویلا
100
Name of Theatre Group
13612
FFL 2023-2024 rule changes
11619
Mountaineering Society Events Survey
10528
Assistance From Guidance Counselors and Effect On School Grades
14725
Trauma in Law Enforcement
6349